perfectlab / Shutter
perfectlab / Shutter
Die vermoë om veroudering te keer, is iets wat baie mense in hul leeftyd wil sien. Dit is nog ver van die werklikheid, maar in ons nuutste eksperiment het ons die veroudering van menslike selle omgekeer, wat die basis kan bied vir toekomstige anti-degenerasie middels.
Veroudering kan beskou word as die progressiewe afname in liggaamlike funksie en word gekoppel aan die meeste van die algemene chroniese siektes waaraan mense ly, soos kanker, diabetes en demensie. Daar is baie redes waarom ons selle en weefsels ophou funksioneer, maar 'n nuwe fokus in die biologie van veroudering is die ophoping van "senescent" selle in die weefsels en organe.
Senescent selle is ouer verswakte selle wat nie funksioneer soos hulle behoort nie, maar ook die funksie van selle rondom hulle kompromitteer. Verwydering van hierdie ou disfunksionele selle was gewys om te verbeter baie eienskappe van veroudering in diere soos die vertraagde aanvang van katarakte.
Ons verstaan steeds nie ten volle waarom selle senescent word soos ons ouderdom het nie, maar skade aan DNA, blootstelling aan inflammasie en beskadiging van die beskermende molekules aan die einde van die chromosome - die telomere - is almal voorgestel.
Meer onlangs het mense voorgestel daardie een bestuurder van senesensie kan die verlies van ons vermoë wees om gene op en af te skakel op die regte tyd en op die regte plek.
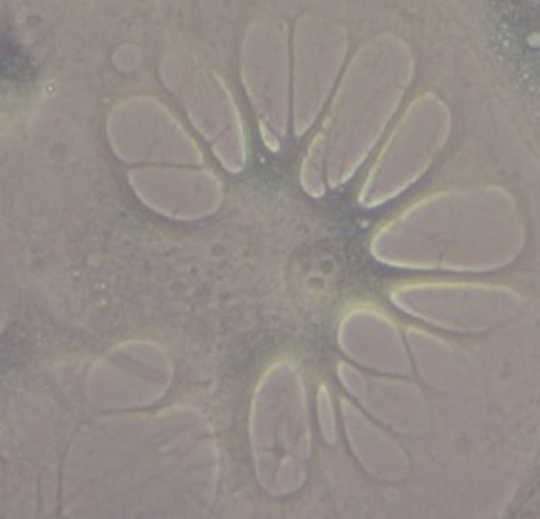
'N Senescent sel. Eva Latorre, skrywer met dien verstande
Een geen, baie boodskappe
Soos ons ouderdom verloor, verloor ons ons vermoë om te beheer hoe ons gene gereguleer word. Elke sel in die liggaam bevat al die inligting wat nodig is vir die lewe, maar nie alle gene word aangeskakel in alle weefsels of onder alle toestande nie. Dit is een van die maniere waarop 'n hartsel van 'n niersel verskil, ten spyte van die feit dat hulle dieselfde gene bevat.
Wanneer 'n geen geaktiveer word deur seine van binne of buite die sel, maak dit 'n molekulêre boodskap (genoem 'n RNA) wat al die inligting bevat wat nodig is om te maak wat die een maak. ons weet nou dat meer as 95% van ons gene eintlik verskillende soorte boodskappe kan maak, afhangende van die behoeftes van die sel.
'N Goeie manier om hieraan te dink, is om elke gen as 'n resep te oorweeg. Jy kan ook 'n vanielje spons, of 'n sjokoladekoek maak, afhangende van of jy die sjokolade insluit. Ons gene kan so werk. Die besluit oor watter tipe boodskap op enige gegewe tydstip geproduseer word, word gemaak deur 'n groep van ongeveer 300-proteïene wat "splicing factors" genoem word.
Soos ons ouderdom het, is die hoeveelheid splicing faktore wat ons kan verminder. Dit beteken dat ouderdomme selle minder in staat is om gene aan en af te skakel om te reageer op veranderinge in hul omgewing. Ons en ander het getoon dat die vlakke van hierdie belangrike reguleerders afname in bloedmonsters van bejaarde mense, en ook in geïsoleerde menslike senescent selle van verskillende weefseltipes.
Verjonging van ou selle
Ons het maniere gesoek om die splicing faktore weer aan te pas. In ons nuwe werk, het ons getoon dat ons ou selle met 'n chemiese middel wat klein hoeveelhede waterstofsulfied vrystel, behandel, ons vlakke van sommige splytingsfaktore kan verhoog en ou menslike selle kan verjong.
Waterstofsulfied is 'n molekuul wat natuurlik in ons liggame gevind word en dit is getoon verbeter verskeie funksies van ouderdomverwante siekte in diere. Maar dit kan giftig wees in groot hoeveelhede, so ons moes 'n manier vind om dit direk aan die deel van die sel te lewer waar dit nodig is.
Deur die gebruik van 'n "molekulêre poskode" kon ons die molekule lewer direk na die mitochondria, die strukture wat energie in selle produseer, waar ons dink dit werk, laat ons toe om klein dosisse te gebruik, wat minder geneig is om newe-effekte te veroorsaak.
![]() Ons is hoopvol dat ons in die gebruik van molekulêre gereedskap soos hierdie, senescentelle in lewende mense sal verwyder, wat ons in staat sal stel om verskeie ouderdomverwante siektes gelyktydig te rig. Dit is een of ander manier in die toekoms, maar dit is 'n opwindende begin.
Ons is hoopvol dat ons in die gebruik van molekulêre gereedskap soos hierdie, senescentelle in lewende mense sal verwyder, wat ons in staat sal stel om verskeie ouderdomverwante siektes gelyktydig te rig. Dit is een of ander manier in die toekoms, maar dit is 'n opwindende begin.
Oor Die Skrywer
Lorna Harries, Medeprofessor in Molekulêre Genetika, Universiteit van Exeter en Matt Whiteman, professor van eksperimentele terapeutiese middels, Universiteit van Exeter
Hierdie artikel is oorspronklik gepubliseer op Die gesprek. Lees die oorspronklike artikel.
Verwante Boeke:
at InnerSelf Market en Amazon