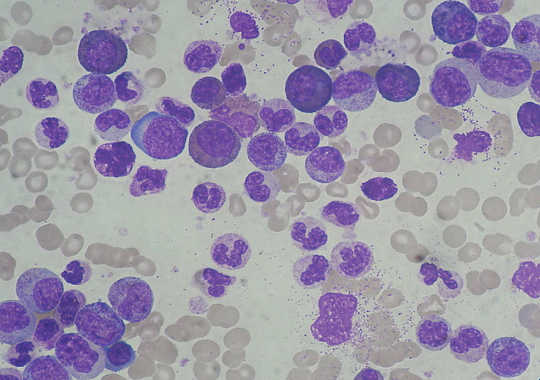
 Chroniese Myeloïde Leukemie smeer. Paulo Henrique Orlandi Mourao via Wikimedia Commons., CC BY-SA
Chroniese Myeloïde Leukemie smeer. Paulo Henrique Orlandi Mourao via Wikimedia Commons., CC BY-SA
Gesonde selfunksie maak staat op goed georkestreerde geenaktiwiteit. Via 'n fantasties komplekse netwerk van interaksies, werk 30,000 genes saam om hierdie delikate balans in elk van die 37.2 triljoen selle in die menslike liggaam.
Breedweg, kanker is 'n ontwrigting van hierdie balans deur genetiese veranderinge, of mutasies. Mutasies kan ooraktivering van gene veroorsaak wat normaalweg selle opdrag gee om te verdeel of inaktivering van gene wat die ontwikkeling van kanker onderdruk. Wanneer 'n gemuteerde sel verdeel, slaag dit die mutasie na sy dogterselle. Dit lei tot die ophoping van nie-funksionele, abnormale selle wat ons as kanker herken.
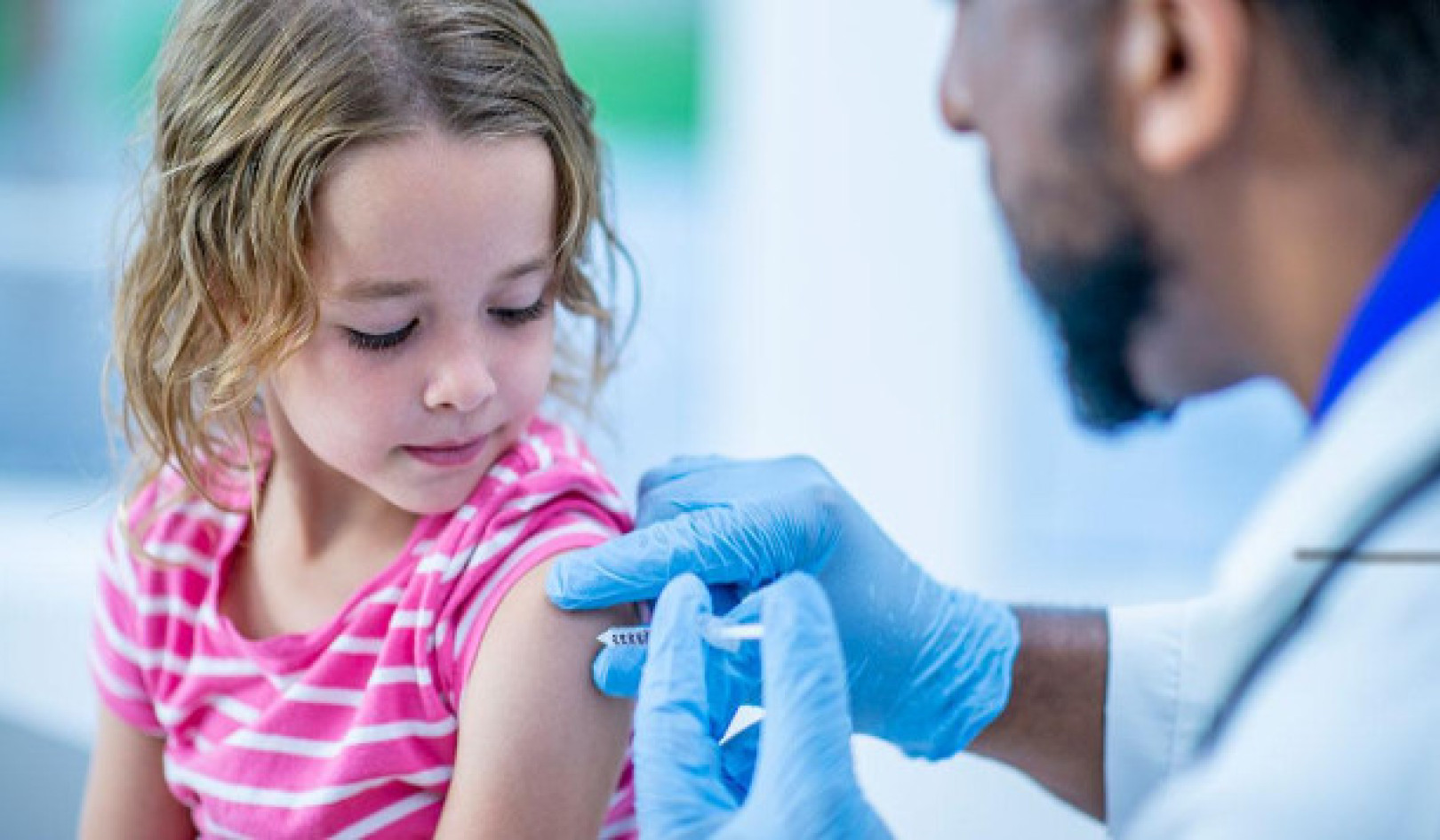
Ons laboratorium is daarop gemik om te verstaan hoe een bepaalde kanker - chroniese myeloïde leukemie of CML - werke. Elke jaar meer as 700 pasiënte in die Verenigde Koninkryk - en oor 100,000 wêreldwyd - word met CML gediagnoseer. Na onlangse vooruitgang, Byna 90% van pasiënte onder die ouderdom van 65 oorleef nou vir meer as vyf jaar.
Maar in die oorgrote meerderheid van pasiënte is CML tans ongeneesbaar en lewenslange behandeling beteken dat pasiënte met newe-effekte moet leef en die kans op dwelmweerstand kan ontstaan. Met toenemende aantal CML-pasiënte wat oorleef (en behandeling kos tussen £ 40,000 en £ 70,000 per pasiënt per jaar), word toenemende spanning op gesondheidsdienste geplaas.
'N Enkele mutasie
CML is dalk uniek in kankers, in die sin dat 'n enkele mutasie genoem word BCR-ABL, onderliggend aan die siekte biologie. Hierdie mutasie ontstaan in 'n enkele leuemiese stamsel, maar word dan deur die bloed en beenmurg gepropageer, aangesien leukemiese selle oorneem en die gesonde proses van bloedproduksie blokkeer. Die teenwoordigheid van BCR-ABL beïnvloed die aktiwiteit van duisende gene, wat weer voorkom dat hierdie selle hul normale funksie as bloed selle vervul.
dwelms wat spesifiek die afwykende effekte van hierdie mutasie neutraliseer, is vanaf die vroeë 2000's aan die kliniek bekendgestel. Hierdie middels het CML pasiënte versorg. Baie is nou in staat om relatief normale lewens te leef met hul leukemie onder goeie beheer.
Maar terwyl hierdie dwelms die meer volwasse dogterselle van die oorspronklik gemuteerde leukemie-stamsel doodmaak, het hulle nie ten volle tot hul aanvanklike faktuur as "magiese kolletjies" in die stryd teen kanker geleef nie. Dit is omdat die oorspronklike "saad" bevolking van leukemiese stamselle ontduikterapie, lê in die beenmurg dormant om nuwe kankergroei te stimuleer wanneer behandeling teruggetrek word.
Om CML regtig te genees, moet ons die innerlike werking van die leukemie-stamcellen ontwrig en ontwrig. En om dit te doen, moet ons meer oor hulle leer. Hoe oorleef hulle die behandeling wat so makliker hul meer volwasse eweknieë doodmaak? Watter ooraktiewe of geïaktiveerde gene beskerm hulle?
Ons glo dat die antwoorde op hierdie vrae lê in die analise van biologiese "groot data". Genoomskaal-tegnologieë laat wetenskaplikes nou die aktiwiteit (of "uitdrukking") van elke geen in die genoom gelyktydig, in enige gegewe populasie van selle, of selfs op die vlak van 'n enkele sel, meet. Vergelyking van uitdrukkingsdata gegenereer uit leukemie stamcellen met dieselfde data wat uit gesonde bloedstamselle gegenereer word, sal enkele genes of netwerke van gene wat potensieel teiken is in die stryd teen leukemie, openbaar.
Groot data tot die redding
In 'n projek befonds deur Bloodwise en die Skotse Kanker Stigting, het ons geskep LEUKomics. Hierdie aanlyn data portaal bring 'n rykdom van CML gene ekspressie data uit gespesialiseerde laboratoriums regoor die wêreld, insluitend ons eie aan die Universiteit van Glasgow.
Ons bedoeling is om die bottelnek uit te skakel wat groot data-analise in CML behels. Elke datastel word onderworpe aan manuele kwaliteitskontrole en al die nodige berekeningsverwerking inligting oor genuitdrukking te onttrek. Dit stel onmiddellike toegang tot en interpretasie van data moontlik wat voorheen nie maklik toeganklik was vir akademici of klinici sonder opleiding in gespesialiseerde berekeningsbenaderings nie.
Deur hierdie data in 'n enkele bron te konsolideer, word ook grootskaalse, computasioneel-intensiewe navorsingspogings deur bioinformatici (spesialiste in die analise van groot data in biologie) toegelaat. Uit 'n rekenaarkundige perspektief, is die feit dat CML deur 'n enkele mutasie veroorsaak word, 'n aantreklike siekte model vir kankerstamselle. Bestaande datastelle is egter geneig om klein steekproefgetalle te hê, wat hul potensiaal kan beperk.
Hoe meer monsters beskikbaar is, hoe hoër is die krag om subtiele veranderinge op te spoor wat noodsaaklik is vir die biologie van die kankerstamselle. Deur al die wêreldwye beskikbare CML-datastelle saam te bring, het ons die steekproefgrootte aansienlik verhoog, van twee tot ses per datastel tot meer as 100. Dit bied 'n ongekende geleentheid om genexpressie data te ontleed om die onderliggende meganismes van hierdie siekte bloot te stel.
Vanaf Maart 2017, die portaal is aan die gang in die publieke domein. Ons beplan om Skotland te toer en teenwoordig op internasionale konferensies, met die doel om navorsers op te lei in hoe om hierdie nuwe hulpbron die beste te benut. Uiteindelik hoop ons dat hierdie instrument nuwe idees en benaderings sal lei en meer befondsing sal trek in die stryd teen CML. En terwyl ons voortgaan om ons verteenwoordiging van CML-data in reële tyd uit navorsingsentrums oor die hele wêreld uit te brei, beplan ons ook om data van ander tipes leukemie in te sluit.
In onlangse jare het geteikende terapieë geword uiters belangrik in kankernavorsing. Deur hierdie data aan die CML navorsingsgemeenskap binne te bied LEUKomics, ons hoop om nuwe navorsing te mobiliseer oor kankerverwekkende leukemiese stamselle en uiteindelik behandelings te ontwerp om hulle te rig sonder om gesonde selle te beïnvloed. Ons databasis bied 'n kritieke stap in hierdie proses.
Oor Die Skrywer
Lorna Jackson, PhD-kandidaat (Paul O'Gorman Leukemia Research Center), Universiteit van Glasgow en Lisa Hopcroft, navorsingsgenoot (Instituut vir Kankerwetenskappe), Universiteit van Glasgow
Hierdie artikel is oorspronklik gepubliseer op Die gesprek. Lees die oorspronklike artikel.
verwante Boeke
at InnerSelf Market en Amazon